Sumber arus listrik
Arus Listrik—Cara Membuat dan Memeliharanya
 Gerakan teratur partikel bermuatan disebut arus listrik. Untuk mendapatkan arus listrik di dalam kawat, Anda perlu membuat medan listrik di dalamnya. Jika benda bermuatan dihubungkan dengan kabel ke tanah, maka arus listrik jangka pendek terjadi di kabel tersebut. Untuk mendapatkan dan mempertahankan medan listrik dalam kawat, gunakan sumber arus listrik.
Gerakan teratur partikel bermuatan disebut arus listrik. Untuk mendapatkan arus listrik di dalam kawat, Anda perlu membuat medan listrik di dalamnya. Jika benda bermuatan dihubungkan dengan kabel ke tanah, maka arus listrik jangka pendek terjadi di kabel tersebut. Untuk mendapatkan dan mempertahankan medan listrik dalam kawat, gunakan sumber arus listrik.
Dalam sumber arus apa pun, pekerjaan dilakukan untuk memisahkan partikel bermuatan positif dan negatif. Partikel yang terpisah menumpuk di kutub sumber. Medan listrik dihasilkan di antara kutub. Jika Anda menghubungkannya dengan kabel, maka medan muncul di kabel.
Pada mesin listrik, pemisahan muatan dilakukan dengan bantuan energi mekanik. Pada saat yang sama, itu menjadi listrik. Dalam termokopel, energi dalam diubah menjadi energi listrik. Baterai nuklir mengubah energi atom menjadi listrik.
Fotosel mengubah energi cahaya menjadi energi listrik. Sel surya terdiri dari fotosel.Mereka digunakan di mana energi cahaya paling mudah tersedia.
Energi sungai, batubara, minyak dan atom diubah menjadi energi listrik di pembangkit listrik. Sumber arus listrik yang paling umum adalah sel galvanik dan baterai.
Sel galvanik
Sel galvanik adalah sumber arus di mana energi kimia diubah menjadi energi listrik.
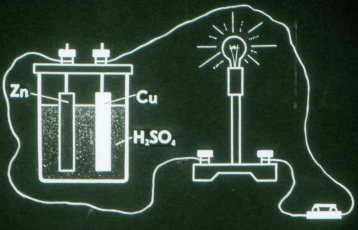
Beginilah cara kerja sel galvanik paling sederhana.
Sel elektrokimia pertama ditemukan oleh Volt pada tahun 1799. Dari elemen-elemen individual ia membuat sebuah baterai yang disebutnya "tiang volt". Dalam sel galvanik, elektroda harus berinteraksi dengan larutan dengan cara yang berbeda, itulah sebabnya elektroda terbuat dari bahan yang berbeda.

Pelat seng dalam sel Volta bermuatan negatif dan pelat tembaga bermuatan positif.
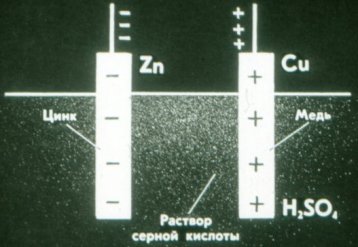
Dan beginilah cara kerja sel galvanik kering. Alih-alih cair, ia menggunakan pasta kental:
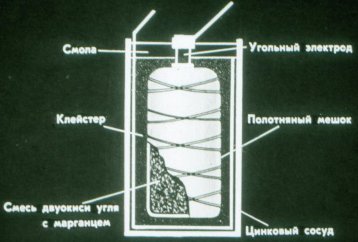
Baterai dapat terdiri dari beberapa elemen:

Bola lampu di lampu listrik, serta berbagai peralatan listrik portabel lainnya dan mainan anak-anak, ditenagai oleh sel galvanik. Ketika elektroda dalam sel galvanik habis, sel diganti dengan yang baru.
Baterai
Baterai adalah sumber arus listrik kimia di mana elektroda tidak dikonsumsi. Baterai paling sederhana terdiri dari dua pelat timah yang dicelupkan ke dalam larutan asam sulfat.
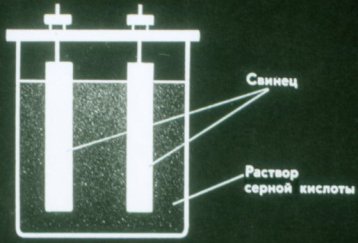
Baterai seperti itu masih tidak mengalirkan arus. Itu harus diisi sebelum digunakan. Untuk melakukan ini, sambungkan kutub baterai ke kutub yang sama dari setiap sumber arus.
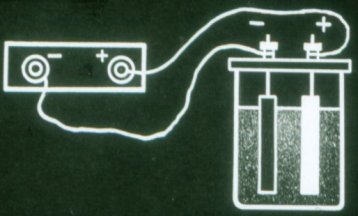
Arus yang mengalir melalui baterai selama pengisian mengubah komposisi kimia pelatnya. Energi kimia baterai meningkat.
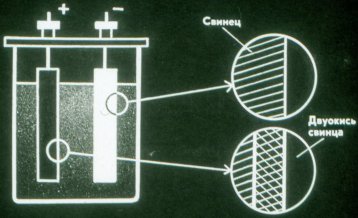
Ketika baterai kosong, itu mengubah energi kimia menjadi energi listrik. Baterai yang habis dapat diisi ulang.
Baterai dikumpulkan dari baterai terpisah.
Selain baterai asam (timbal), baterai alkalin (besi-nikel) juga digunakan.
Baterai Besi Nikel:
Baterai nikel-kadmium dan nikel-logam hidrida juga banyak digunakan saat ini. Baterai perak-seng digunakan dalam penerbangan dan luar angkasa Jenis baterai baru: lithium-ion, lithium-polymer digunakan di ponsel, tablet, dan peralatan portabel modern lainnya.
Baterai digunakan dalam kasus di mana sumber arus listrik lebih menguntungkan untuk diisi ulang daripada mengganti dengan yang baru. Di dalam mobil, aki digunakan untuk menghidupkan mesin dan mengoperasikan berbagai perangkat. Di luar angkasa, baterai diisi oleh panel surya. Saat habis, ini memberi daya pada pemancar dan peralatan radio.
Lihat juga: Baterai. Contoh perhitungan

